Sindromet Mielodisplazike [MDS] përbëjnë një grup heterogjen patologjish malinje klonale të qelizës staminale hematopoietike që karakterizohen nga një hematopoieze joefektive me citopeni e tre linjave qelizore, me një palcë kockore në shumicën e rasteve me celularitet të shtuar dhe me një risk të lartë transformimi në leukemi akute.
Pacientë të tillë prezantohen me një varietet simptomash që përfshijnë aneminë, hemorragjitë apo infeksionet.
Në bazën e patogjenezës së këtyre patologjive qëndrojnë çrregullimet në apoptozë, alterimet citogjenetike si dhe ndryshimet në mikroambientin e palcës kockore.
Ekspansioni klonal i limfociteve T citotoksike, dhe reagimi ndaj mjekimit me terapi imunosupresore i një pjese pacientësh me MDS sugjeron se kemi të bëjmë me mekanizma autoimune që luajnë rol gjithashtu në patogjenezën komplekse të mielodisplazive.
Sindromet Mielodisplazike shpeshherë janë të shoqëruara me manifestime klinike të sëmundjeve autoimune si dhe me prani të reaksioneve inflamatore.

Po ashtu janë gjetur antikorpet antinukleare me titra të lartë në pacientët me MDS pa pasur prezent praninë e një sëmundjeje autoimune në aktivitet.
Në një nëngrup pacientësh me MDS mendohet se citopenia që paraqesin të jetë pasojë e pikërisht e këtij aktiviteti autoimun, pasojë e çlirimit në titra shumë të lartë e citokinave inflamatore siç faktori i nëkrozës tumorale [TNF-α] dhe i interferonit [IF-γ] që nxisin apoptozën e prekursorëve mieloide duke sjellë citopeni.
Po ashtu prezantimi për herë të parë me trobocitopeni imune apo dhe me anemi hemolitike autoimmune në një pjesë pacientësh me MSD flet se në patogjenezën e këtij grupi çrregullimesh, autoimuniteti luan një rol të rëndësishëm.
E përshkruar për herë të parë në vitin 1907 nga Luzzato si “anemia pseudo aplastike” dhe më pas në 1949 nga Hamilton-Paterson me termin “anemia preleukemike” për pacientët me anemi refraktare me tendencë transformimi në leukemi akute mieloblastike [LAM], MDS u klasifikua si një grup patologjish vetëm në vitin 1975 (1).
MDS përfaqësojnë një grup çrregullimesh klonale të qelizës hematopoietike staminale të karakterizuar nga një hematopoieze inefektive, citopeni, çrregullime cilësore dhe sasiore të elementëve qelizore në gjakun periferik si dhe të prekursorëve të tyre, dhe me një tendencë variable transformimi drejt leukemisë akute mieloblastike (2).
Është vlerësuar se incidenca e MDS varion nga 10,000 – 15,000 / raste të reja në vit dhe kjo incidencë po rritet me prekje kryesisht të moshave 65 -70 vjec.
Duke qenë se kemi të bëjmë me patologji që prek kryesisht të moshuarit, pyetja shtrohet nëse autoimuniteti është shkak apo pasojë e sindromeve mielodisplazike?
Roli i Autoimunitetit në patogjenezën e MDS
MDS është një grup patologjish klonale malinje që prek zhvillimin e qelizave immature hematopoietike [blastet].
Nisur nga përqindja e blasteve kemi edhe ndarjen e MDS-ve sipas klasifikimit FAB në anemi refraktare me ekces blastesh 1 dhe 2 [AREB-1, AREB-2] dhe mbështetur në numrin e blasteve përcaktohet edhe klasifikimi i pacientëve nëse është MDS apo LAM duke patur si kufi bazë nisur nga klasifikimi sipas WHO numrin e blasteve < 20% në palcën e kockës për MDS.
Në 90% të pacientëve haset një palcë kockore hipercelulare, dhe vetëm në 10% të tyre vërehet një hipocelularitet që duhet diferencuar nga një anemi aplastike[AA](2).
Anomalitë kromozomale dhe epigjenetike të gjendura në AND, apoptoza e përshpejtuar, përgjigjia e dëmtuar ndaj citokinave, dhe angiogjeneza në palcën e kockës e shoqëruar me një çrregullim të stromës së saj janë të gjithë faktorë që gjenerojnë tiparet e ndryshme dhe variabilitetin klinik të MDS (3,4,5).
Përshpejtimi i apoptozës dhe çrregullimi i saj në nivel të progenitorëve përbën edhe pikën kyçe, apo mekanizmin kyç të zhvillimit të MDS-ve që rezulton në krijimin e qelizave “living dead” me morfologji displastike.
Studimet kanë treguar se në palcën e kockave jemi përballë një numri të shtuar qelizash hematopoietike që proliferojnë shumë shpejt, por që po me aq ritme të shpejta i nënshtrohen apoptozës, proces ky i mediatuar nga citokinat siç TNFα, IL-6, IL-1β dhe të tjerë të ngjashëm me to.
Po ashtu prezenca e apoptozës edhe në qelizat stromale si dhe vërejtja e një shpërndarjeje qelizore jo normale në palcën e kockës tregon se kemi të bëjmë edhe me një dëmtim të mikroambjentit dhe me anomali stromale. Studimet kanë demonstruar pikërisht praninë e një prodhimi anormal të citokinave dhe po ashtu një marrëdhënie qelize hematopoietike – strome të dëmtuar (4).
Gjetjet e fundit kanë treguar se MDS mund të jetë një rezultat i një reaksioni autoimun drejtuar qelizave staminale, por kjo ende mbetet një hipotezë për t’u vërtetuar.
Në palcën e kockave gjenden qeliza mediatore të imunitetit dhe veçanërisht lifocitet T, që janë pjesë mikroambjentit dhe marrin pjesë në proliferimin dhe në diferencimin e qelizave hematopoietike.
Pacientët me MDS paraqesin një përqindje të lartë të qelizave T që kanë në sipërfaqen e tyre CD8+, CD28-, CD57+, dhe që përcaktojnë kështu fenotipin e qelizave limfocitare T citotoksike. Por këto qeliza janë gjetur edhe në situata të tjera autoimmune.
Këto qeliza kanë një prezantim të kufizuar receptorësh duke sugjeruar në këtë mënyrë se kemi të bëjmë me një ekspansion klonal dominant T qelizor. Por jo detyrimisht një ekspansion klonal do të thotë malinjance, pasi mund të përfaqësojë edhe ekspansion klonal apo oligoklonal qelizash T autoreaktive.
Pra në këtë mënyrë, prania shtuar e CD57+ në qelizat T me ekspresion të CD8+ haset në një ambjent me aktivizim të imunitetit , psh në graft versus host disease [GVHD], në sklerozën multiple, dhe madje edhe në artritin rheumatoid(6).
Një studim prospektiv ka evidentuar manifestime autoimmune inflamatore në 22% të pacientëve me MDS duke i dhënë suport idesë se autoimuniteti luan një rol kyç në MDS(7).
Sëmundjet autoimmune dhe MDS
Sindromet Mielodisplazike shoqërohen shpesh me manifestime klinike të sëmundjeve të ndyshme autoimmune. Për shembull është parë që janë të shoqëruara me vaskulitin leukocitoklastik, periarteritin nodoz, mikropoliangeitin, polikondritin në relaps, Sweet syndrome, me poliarteritin seronegativ dhe madje hasën në mënyrë frekuente ANA positive, por pa shfaqje të dukshme klinike të sëmundjeve autoimmune.
Është parë se në një grup pacientësh me MDS citopenia të jetë një pasojë e një aktiviteti imun autoreaktiv, dhe kjo shpjegon reagimin pozitiv që kanë këta pacientë ndaj përdorimit të mjekimit me imunosupresore.
Anemia refraktare me ekces të blasteve (AREB), AREB që transformohet drejt leukemisë acute si dhe leukemia mielomonocitare kronike (CMML) janë veçanërisht të shoqëruara me këto fenomene e sidomos me Sweet Syndrome e cila është parë se haset në 10% të rasteve me MDS dhe me LAM.
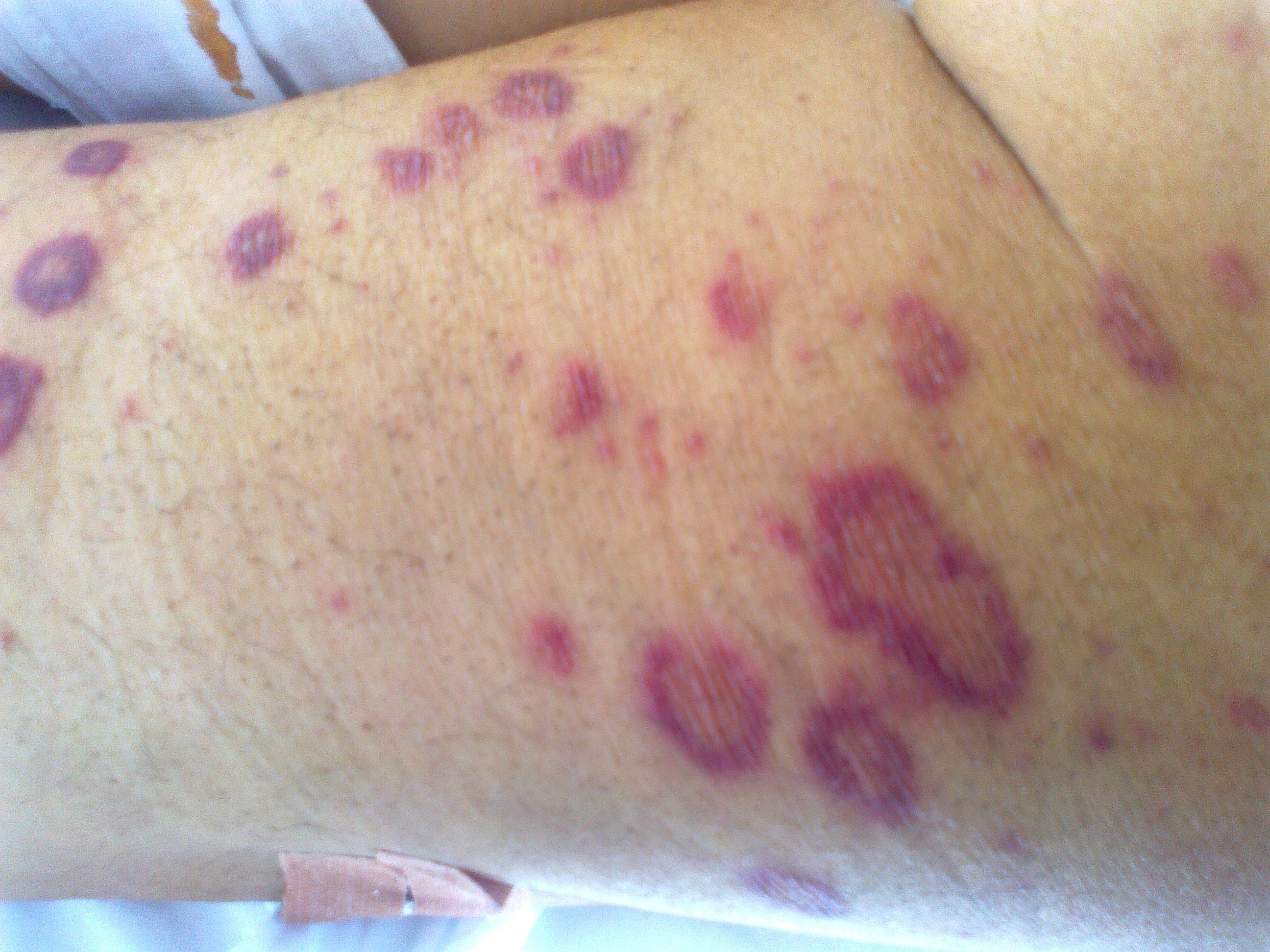
Figura 1: Pacientja N.G, 68-vjece. Sweet syndrome si shenjë e parë e prezantimit të AREB-2 e cila më pas u transformua në LAM. Imazh nga A.Perolla.
Zakonisht terapia me kortikosteroide është mjaft efikase, por është parë se përdorimi i preparative imunosupresore i shton komplikacionet infektive dhe po ashtu është parë një shtim i riskut të transformimit drejt leukemisë akute.
Është parë se MDS shoqëron në 40% të rasteve një polikondriti në relaps dhe kjo është hasur në pacientë me moshë mbi 60 vjeç.
Po ashtu është parë se një pjesë e pacientëve me MDS paraqesin si shenjë të parë një anemi hemolitike autoimmune me test coombsi direct dhe indirect pozitiv. Po ashtu është raportuar gjetje e Morbus Behcet në korelacion me pacientë me MDS që kanë trisomi 8. Megjithatë mekanizmat pse vërehet një gjetje e tillë ende mbeten për t’u sqaruar.
Konkluzion
Si përfundim, marrëdhënia që vërehet midis sëmundjeve autoimmune dhe sindromeve mielodisplazike mbetet ende për t’u sqaruar dhe për këtë nevojiten studime të mëdha me një numër të madh pacientësh për të përcaktuar saktë se cili është roli i autoimunitetit në zhvillimin e insuficiencës së palcës së kockës dhe me çfarë mekanizmash luan rol ai në progresin e MDS drejt leukemisë akute.
Referencat:
1. List AF in Wintrobe’s Clinical Hematology copyright 2003 Lee RG Wiliams&Williams.
2. Hofmann WK, Lubbert M, Hoelzer D, Koeffler PH. Myelodysplastic syndromes. Hemtol J 2004;5(1):1-8
3. List AF. New approaches to the treatment of Myelodysplasia. Oncologist 2002;7, suppl. 1:39-49
4. Parker JE and Mufti GJ. The myelodysplastic syndromes: a matter of life and death. Acta Haematol 2004;111(1-2):78-99
5. Cilloni D, Messa E, messa F, Carturan S, Defilippi I, Arruga F, Rosso V, Catalano R, Bracco E, Nikoli P, Saglio G. Genetic abnormalities as target for molecular therapies in myelodysplastic syndromes. Ann NY Acad Sci.2006;1098: 411-23
6. Martin Stern, Andreas S Buser, Andreas Lohri, Andre Tichelli, Catherine Nissen – Druey. Autoimmunity and malignancy in hematology.- more than an association.Crit Rev in Onc/Hematol 2007;63:100-110
7. S Giannouli, M Voulgarelis, E Zintrazas : Autoimmune phenomena om myelodysplastix syndromes : a 4-year prospective study. 2004 Reumatology;43:626-32
8. Braun T, Fernaux P. myelodysplastic syndromes (MDS) and autoimmune disorders(AD0: cause or consequence?. Best Pract Res Clin Haematol.2013 dec:26(4):327-36
9. Fain O, Braun T, Stirnemann J, Fenaux P. Systemic and autoimmune manifestations in myelodysplastic syndromes. Rev Med Interne 2011 Sep;32(9): 552-9
10. Chamuleau MED, Westers TM, vanDreunen L, Groenland J, Zevenbergen A, Eeltink CM,et al. Immune mediated autologous cytotoxicity against hematopoietic precursor cells in patients with myelodysplastic syndrome.
Haematologica 2009;94:496–506.
Adela Perolla






















